
Elemento químico de la tabla periódica que fue descubierto en 1817 por el químico de nacionalidad sueca llamado Jöns Jakob Berzelius en un residuo de ácido sulfúrico donde observo un líquido rojizo que al calentarlo desprendía un olor desagradable que antes solo se le atribuía al telurio, después de sus investigaciones resulto el descubrimiento del selenio. Su nombre fue dado de acuerdo a su relación al telurio, ya que telurio viene del latín Tellus y al selenio se le asigno su nombre que viene del griego Selene que significa Luna.
El selenio se encuentra en el planeta Tierra, distribuido en la corteza terrestre, en su mayoría rocas y suelos, con una abundancia de entre 0.1 y 0.2 ppm (partes por millón) en forma de seleniuros de elementos pesados, también se puede encontrar como elemento libre en asociación con Azufre elemental aunque en menores cantidades.
La fuente principal de obtención de Selenio son los minerales de sulfuro de cobre seleníferos ya que los minerales de selenio no se encuentran en suficientes cantidades como para tener utilidad comercial.
Los recursos de Selenio que se encuentran asociados a los depósitos de cobre conocidos hasta ahora son aproximadamente de 170 000 toneladas, aunque se calcula que existen aún otras 425 000 toneladas en más depósitos de cobre y otros metales pero que aún no han sido explotados por el hombre.
El Selenio también se encuentra en el carbón, entre 0.5 y 12 ppm que equivale a unas 80 o 90 porciento más de lo que se encuentra en las menas de cobre pero su separación del carbón aún no se ah podido realizar.
Su obtención para ser comercializado se realiza por tostación de cenizas de sosa o ácido sulfúrico de los lodos y se realiza de la siguiente manera:
- se añade un aglomerante de cenizas de sosa y agua a los lodos para formar una pasta que se corta en partes para seguir con el secado.
- la pasta se tuesta a altas temperaturas ( 550 – 650 grados Celsius) y se sumerge en agua para obtener selenio hexavalente que se disuelve como un selenato de sodio (Na2SeO4).
- el selenato se reduce a seleniuro, calentándose y obteniendo una solución de color rojo.
- después se le inyecta aire para que se oxide la solución y así poder obtener el selenio.
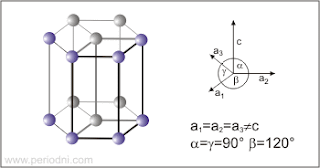
El selenio tiene una estructura cristalina hexagonal, es de color gris con una densidad de 4,81 g/cm3, masa de 78.96 gramos por mol, radio atómico de 116 picómetros.
Cuenta con 34 electrones (número atómico).
Su configuración electrónica es de [Ar] 3d10 4s2p4 su electronegatividad es de 2.55. Tiene un punto de fusión de 494 K y su punto de ebullición es de 957.8 K.
Se encuentra en el cuarto periodo de la tabla periódica, en la familia del Oxigeno, en un no metal y su estado de la materia es sólido. En insoluble en agua y alcohol.
El Se tiene una serie de isótopos entre los cuáles los isótopos estables son:
- 74Se
- 76Se
- 77Se
- 78Se
- 80Se
- 82Se
Este elemento tiene un rol biológico muy importante, en un micronutriente y se encuentra en el pan, cereales, pescado carne y huevo.
Además es un antioxidante que nos ayuda a neutralizar los radicales libres e interviene en el buen funcionamiento de la glándula tiroides.
En investigaciones también se ah encontrado que ayuda a la prevención de cáncer en los humanos.
Es por eso que en nuestra dieta debe estar incluido el Selenio y no es muy difícil de hacerlo ya que esta presente en varios alimentos de consumo diario.
La deficiencia de selenio es muy rara pero si se da sobre todo en pacientes con disfunción intestinal o en poblaciones donde los alimentos vienen de cultivos que se encuentran en suelos que tienen concentración muy baja de Selenio.
Aún así si la ingesta de selenio es mayor a la recomendada puede provocar efectos tóxicos.
Además de la importancia biológica, el selenio tiene otras aplicaciones en campos diferentes tanto electrónicas y eléctricas, también se usa en la fotografía e incluso se usa como un catalizador en reacciones de deshidrogenación.
- en la fotografía se usa para intensificar el rango de tonos de las fotografías y la durabilidad de estas.
- El seleniato de sodio se usa como insecticida y en el campo de la medicina para el control de enfermedades animales.
- El sulfuro de selenio se usa en el tratamiento de la caspa, el acné, dermatitis seborreica y otras enfermedades de piel.
- El selenito de sodio se usa en la industria del vidrio y como aditivo para suelos pobres en selenio y el selenito de amonio en la fabricación de vidrio y esmalte rojos.
- También se le agrega selenio al caucho vulcanizado para así aumentar su resistencia al desgaste.
- El selenio también se usa en fotocopiadoras, semiconductores, aleaciones,
células solares y rectificadores.
Como se pudo ver el selenio es un elemento que cuenta con varias aplicaciones en campos diferentes y su abundancia es grande en la corteza, así que este elemento se podría trabajar de diferentes maneras y así tener un mejor aprovechamiento.



2 comments:
muy buena la info, espero que sea veraz. gracias
¿Como se podría obtener el Selenio tanto a nivel industrial como en laboratorio?
Post a Comment